MINISTÉRIO DA SAÚDE EM SILÊNCIO
Infarmed autorizou uso de vacinas (contra a covid-19) fora do prazo de validade, e contrariando normas dos fabricantes.
No Alentejo, foram administradas a um número indeterminado de pessoas vacinas contra a covid-19 fora do prazo. A decisão foi tomada no passado mês de Março em articulação entre o Infarmed e a Administração Regional de Saúde daquela região, mas sem base legal e contra as normas dos fabricantes. Apesar de garantir ser um processo seguro, o Infarmed acabou por estabelecer a obrigatoriedade de recolha de informação sobre as pessoas injectadas com estes lotes para posterior avaliação de eventuais acréscimos dos efeitos adversos ou de redução da efectividade vacinal. O PÁGINA UM revela os lotes das vacinas da Pfizer e da Moderna que foram injectadas já depois de expirar o prazo de validade. O Ministério da Saúde (ainda) não comentou se sabia desta decisão nem esclareceu (ainda) se houve mais lotes fora do prazo usados em outras regiões do país.
O Infarmed autorizou o uso de três lotes de vacinas contra a covid-19 fora do prazo de validade em centros de vacinação do Alentejo durante o mês de Março e Abril, em condições que aparentam um ensaio clínico não autorizado, que não cumpre os mínimos princípios éticos e de consentimento informado.
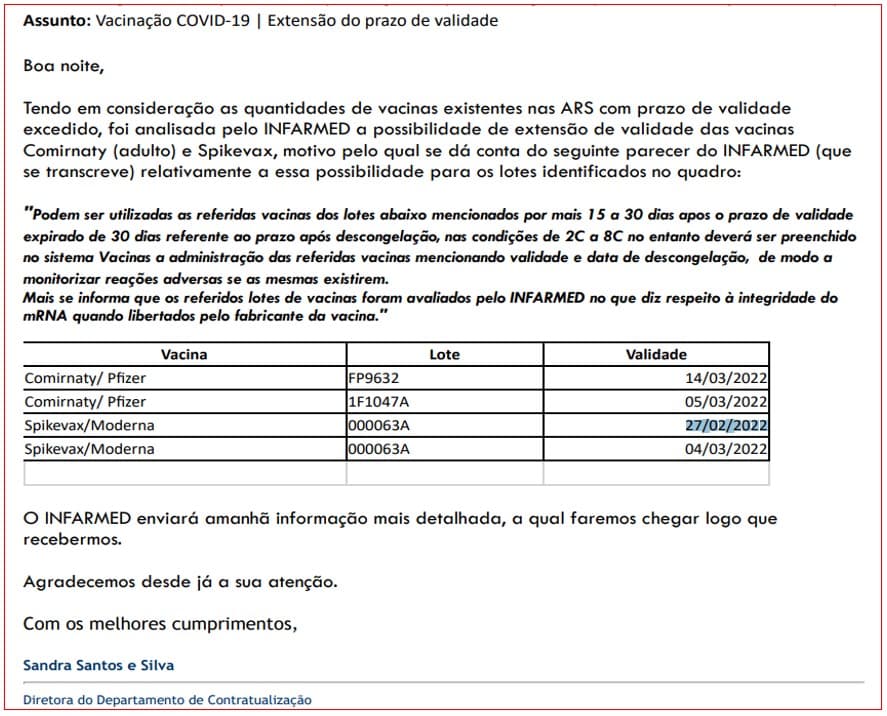
De acordo com mensagens electrónicas a que PÁGINA UM teve acesso, na noite de 14 de Março passado a directora do Departamento de Contratualização da Administração Regional de Saúde (ARS) do Alentejo, Sandra Silva, informou diversos responsáveis daquela região que “tendo em consideração as quantidades de vacinas existentes nas ARS com prazo de validade excedido”, o Infarmed tinha autorizado a sua utilização.
Em causa estava um número indeterminado de frascos dos lotes FP9632 e 1F1047A da vacina Comirnaty/Pfizer, com prazo de validade até 14 de Março e 5 de Março, respectivamente, e ainda um lote 000063A da vacina Spikevax/Moderna, sendo que alguns frascos tinham expirado o prazo de validade em 27 de Fevereiro e outros em 4 de Março. ↓
O jornalismo independente (só) depende dos leitores.
Não dependemos de grupos económicos nem do Estado. Não fazemos fretes. Fazemos jornalismo para os leitores, mas só sobreviveremos com o seu apoio financeiro.
No e-mail daquela noite, além de acrescentar que seria enviada no dia seguinte “informação mais detalhada”, Sandra Silva transcrevia o parecer do Infarmed, constituído somente por duas frases escritas em português algo macarrónico: “Podem ser utilizadas as referidas vacinas dos lotes abaixo mencionadas por mais 15 a 30 dias apos o prazo de validade expirado de 30 dias referente ao prazo após descongelação, nas condições de 2C a 8C no entanto deverá ser preenchido no sistema Vacinas a administração das referidas vacinas mencionando validade e data de descongelação, de modo a monitorizar reações adversas se as mesmas existirem. Mais se informa que os referidos lotes de vacinas foram avaliados pelo Infarmed no que diz respeito à integridade do mRNA quando libertadas pelo fabricante da vacina”.
No site do Infarmed não consta qualquer aviso sobre esta matéria. Sobre as condições de conservação das vacinas covid-19, a última actualização é de 3 de Fevereiro deste ano, onde nada consta sobre a possibilidade de alargamento do prazo de validade.
E no Portal Infomed, e no caso do resumo das características do medicamento da vacina Comirnaty/Pfizer, além de se elencar de forma exaustiva as exigentes condições de conservação, salienta-se que, após descongelação, “os frascos para injectáveis por abrir podem ser conservados durante um total de 10 semanas a uma temperatura entre 2 oC e 8 oC, nunca ultrapassando o prazo de validade (VAL) impresso”.
No caso especifico da Spikevax/Moderna, o resumo das características do medicamento no Portal Infomed vão no mesmo sentido: “Não utilize esta vacina após o prazo de validade impresso no rótulo após VAL [prazo de validade]. O prazo de validade corresponde ao último dia do mês indicado”.
Em todo o caso, nunca fazendo referência às indicações dos fabricantes, na manhã do passado dia 15 de Março, a directora de Inspecção e Licenciamentos do Infarmed, Maria Fernanda Ralha, enviou um e-mail para ARS do Alentejo, explicitando melhor a “autorização” concedida.

Na mensagem aquela responsável do Infarmed garantia que “os referidos lotes das vacinas Comirnaty adulta e Spikevax mantém-se estáveis assumindo-se que nenhuma das outras condições de conservação/transporte aprovadas foi excedida [e que] poderão eventualmente se manter , por mais 15-30 dias, para além da validade aprovada quando as vacinas forem mantidas entre 2ºC e 8ºC desde a sua descongelação” (sic).
Maria Fernanda Ralha sugeria também que, “pela natureza destas vacinas COVID-19 e pelos dados de estabilidade disponíveis para outros lotes”, não se antevia para estes lotes fora de prazo “problemas de segurança”, mas em seguida acrescentava que “há no entanto que estar atentos a eventuais notificações de reações adversas em utentes que receberão estas doses pelo que é recomendado o registo deste desvio às condições aprovadas na plataforma Vacinas”. (sic)
Nessa medida, esta responsável do Infarmed acabou por instruir os responsáveis da ARS do Alentejo para tomarem obrigatórios “procedimentos, tendo em conta a salvaguarda da saúde pública”, entre os quais o registo na plataforma Vacinas da data de descongelação e administração da dose da vacina fora de prazo, de modo a ser possível uma “futura avaliação da efetividade vacinal e eventuais questões de farmacovigilância decorrentes destes desvios”.
Ou seja, assumia subliminarmente que não existiam certezas sobre a inocuidade do prolongamento do prazo de validade nem tão-pouco se ficaria afectada a protecção vacinal.
Esta decisão do Infarmed e da ARS do Alentejo não se deveu a qualquer quebra de stock de vacina. Pelo contrário, tem sido a fraca adesão às doses de reforço, sobretudo da população abaixo dos 50 anos, que tem causado “sobras” e, portanto, risco de partes de lotes expirarem o respectivo prazo de validade. Tanto assim é que a responsável do Infarmed recomendou que “as vacinas descongeladas e cujo prazo de validade aprovado já foi ultrapassado devem ser usadas antes de vacinas descongeladas em qualquer uma das datas subsequentes e só quando terminar o stock existente se passe para as vacinas descongeladas noutros dias”. (sic)
O PÁGINA UM contactou Maria Fernanda Ralha, directora de Inpecção e Licenciamentos do Infarmed, que não quis fazer comentários sobre este assunto, alegando estar de férias e que todas as informações respeitantes às vacinas contra a covid-19 deveriam ser fornecidas pela Direcção-Geral da Saúde.
Também o gabinete da ministra da Saúde, Marta Temido, foi questionado sobre se tinha conhecimento desta decisão do Infarmed e da ARS do Alentejo, e sobre quantas pessoas tinham sido vacinadas com vacinas fora do prazo de validade. E também se questionou o Ministério da Saúde sobre se noutras regiões se tinha usado similar procedimento, e se sim, se este procedimento seria mantido no futuro. Não houve, até agora, qualquer reacção.
