REGULADOR DO MEDICAMENTO NÃO FAZ MONITORIZAÇÃO E ESCONDE INFORMAÇÃO
Infarmed abandona à sua sorte centenas de adolescentes e jovens adultos com reacções graves à vacina contra a covid-19
Começam agora a desvendar-se os verdadeiros motivos para o Infarmed – e sobretudo o seu presidente Rui Santos Ivo, com a conivência do Ministério da Saúde – ter lutado 30 meses para evitar o acesso legal do PÁGINA UM ao Portal RAM, onde constam as notificações das reacções adversas às vacinas contra a covid-19. Mesmo estando a esconder ainda um vasto conjunto de dados (não surgem reacções adversas em crianças dos 5 aos 12 anos) e diversas variáveis, em incumprimento de um acórdão do Tribunal Central Administrativo do Sul, o PÁGINA UM já detectou mais de 225 casos graves afectando menores de 25 anos, incluindo adolescentes e mesmo recém-nascidos, cuja evolução não teve qualquer acompanhamento pelo Infarmed, desconhecendo-se assim se recuperaram ou se houve um desfecho fatal. Ou seja, o Infarmed regista os casos, mas não faz qualquer monitorização, minando assim a confiança na farmacovigilância. Há reacções com evolução ignorada em casos gravíssimos, incluindo trombocitose, tromboembolismo, miocardite e pericardite, embolia pulmonar, trombose venosa cerebral, trombocitopenia imune e acidente vascular cerebral. O Infarmed e o Ministério da Saúde, confiantes num (quase certo) impacte nulo desta investigação na imprensa ‘mainstream’, nem sequer reagiram quando confrontados para comentar as falhas da farmacovigilância que desvirtua uma avaliação da segurança das vacinas sempre ‘vendidas’ como seguras e eficazes.
Uma coisa é a teoria; outra a prática. A farmacovigilância – como dirão, por certo, a ministra da Saúde, Ana Paula Martins, que foi professora universitária na Faculdade de Farmácia da Universidade de Lisboa, ou mesmo o presidente do Infarmed, Rui Ivo – é uma ciência relacionada com a recolha, detecção, avaliação, monitorização e prevenção de efeitos adversos com produtos farmacêuticos. Vem nos manuais, consta das normas legais e procedimentos – é uma imposição, já padronizada após alguns escândalos passados, que surge quando os medicamentos, depois de aprovados seguindo os ensaios clínicos, são colocados no mercado.
E é aí que está em jogo muita coisa: há a perspectiva de um negócio lucrativo legítimo assente na confirmação da eficácia no tratamento ou prevenção de alguma doença ou maleita, mas também o risco de, através dos procedimentos de farmacovigilância, serem detectados efeitos adversos graves que obriguem a limitar o seu uso ou, pior ainda, obriguem à sua retirada pelo facto de os eventuais benefícios não compensarem os riscos.
Não é fenómeno frequente, mas também não é raro. Há quatro anos, num artigo científico publicado na revista Current Drug Safety, quatro investigadores portugueses apresentam uma resenha sobre o processo de decisão, baseado em dados, que tinham levado à retirada do mercado de medicamentos por razões de segurança, sustentando que muitos dos problemas não tinham sido detectados nos processos de pesquisa e desenvolvimento, até porque muitas reacções adversas têm uma incidência que não permite o seu conhecimento em ensaios clínicos que usam poucos milhares de pessoas. ↓
O jornalismo independente (só) depende dos leitores.
Não dependemos de grupos económicos nem do Estado. Não fazemos fretes. Fazemos jornalismo para os leitores, mas só sobreviveremos com o seu apoio financeiro.
O artigo destes investigadores – e existem centenas de artigos similares – chama sobretudo a atenção para o reforço da monitorização – mesmo nos dias de hoje em que a Ciência assume um papel de dogma apenas acessível a ‘peritos’ reconhecidos. Os problemas com medicamentos podem já ter sido piores – por exemplo, 10,2% das novas substâncias activas moleculares introduzidas nos Estados Unidos entre 1975 e 1999 foram retiradas ou levaram a restrições de uso por razões de segurança. Mas continuam a ser reais, e difíceis de assumir, porque há muito a perder.
Por um lado, as farmacêuticas não apenas perdem lucros futuros como podem sofrer elevados pedidos de indemnização. Por outro lado, em casos de escândalo, as autoridades políticas e administrativas tendem a não reconhecer de imediato os erros – porque a farmacovigilância é da sua responsabilidade – e prolongam a tomada de uma posição mais radical. O atraso entre a introdução do medicamento e a sua retirada por razões de segurança, bem como as metodologias usadas para identificar riscos anteriormente desconhecidos.

Diversos estudos mostraram que entre 82% e 90% dos problemas de segurança identificados em medicamentos retirados do mercado foram reconhecidos através de relatos de casos das reacções adversas de medicamentos (RAM). Mas, globalmente, o tempo médio até à retirada é de 20,3 anos, como se destaca no artigo dos quatro investigadores portugueses.
Antes da pandemia da covid-19, que veio introduzir um programa de vacinação maciço jamais visto, mesmo as vacinas eram alvo de uma atenção especial da farmacovigilância. E são conhecidos diversos casos mais ou menos recentes de retirada total ou parcial na Europa e/ ou em outras partes do Mundo por razões de segurança, como a vacina Pandemrix fabricada pela GlaxoSmithKline durante a pandemia de gripe suína de 2009-2010, a da vacina LYMERrix, fabricada contra a doença de Lyme pela actual GSK. Num relatório da Organização Mundial da Saúde relativo ao período 2010-2018 intitulado “Restrictions in use and availability of pharmaceuticals” surgem referidas nove vacinas sobre as quais penderam retiradas ou restrições de uso.
Mas apesar das vacinas contra a covid-19 terem sido o fármaco mais administrado num curto espaço de tempo, incluindo a grupos etários de baixíssimo risco e a pessoas já com imunidade adquirida, as autoridades e os ‘peritos’ sempre recusaram admitir a dimensão das reacções adversas, apontando sempre com a sua alegada eficácia no controlo da pandemia. Mesmo nos relatórios de farmacovigilância dedicados exclusivamente às vacinas contra a covid-19, o Infarmed – seguindo a filosofia das suas congéneres – relativizava os números e os efeitos adversos. Por exemplo, invariavelmente, nos seus relatórios de farmacovigilância – que deveriam ser neutros, prudentes e equidistantes –, o regulador do medicamento português assumia, à partida, que “diversos estudos comprovam que as vacinas contra a covid-19 são seguras e efectivas”. E a partir daí a sua análise estava logo comprometida por um enviesamento ’ideológico’.
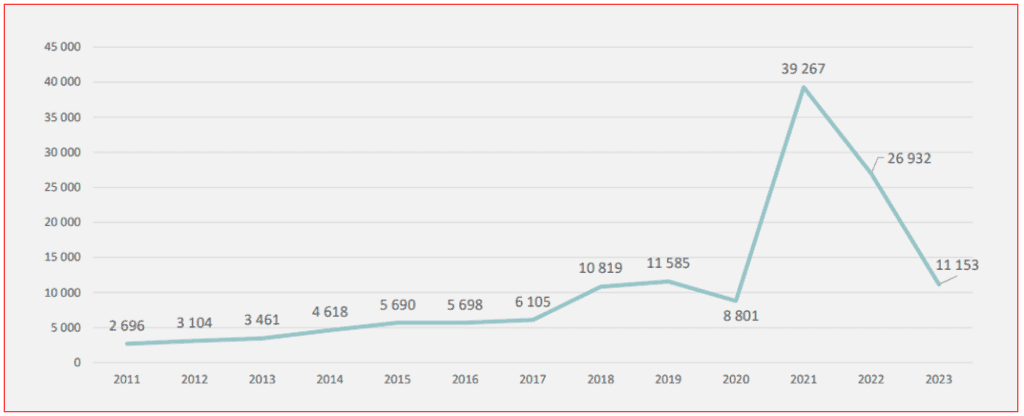
Aliás, tal como a Agência Europeia do Medicamento, também o Infarmed sempre menorizou a catadupa de reacções adversas que foram sendo encaminhadas para os sistemas de farmacovigilância por causa das vacinas contra a covid-19, que passaram a ser, de muto longe, o fármaco com maior número de notificações. Num recente, e bastante simplificado relatório, com apenas 20 páginas, o Infarmed apresenta um gráfico bastante elucidativo sobre o ‘impacte’ das vacinas contra a covid-19. Apesar da tendência de crescimento desde 2011 das notificações de reacções adversas às centenas de medicamentos ‘controlados’ pelo Infarmed, a média anual no triénio anterior à pandemia (2017-2019) situou-se em 9.503.

No primeiro ano da pandemia, em 2020, e sabendo-se que as vacinas contra a covid-19 somente começaram a ser administradas em 27 de Dezembro, as notificações de reacções a todos os medicamentos até foi ligeiramente inferior: 8.801. Mas depois saltaram para as 39.267 notificações em 2021, descendo para 26.932 no ano seguinte. Em 2023, reflectindo a fraca adesão aos boosters da vacina contra a covid-19, o total de notificações para todos os fármacos desceu para níveis dos anos pré-pandemia, tendo sido contabilizadas 11.153.
Porém, neste relatório de qualidade bastante sofrível, pela ausência de detalhe, o Infarmed nem sequer discrimina os fármacos associados às reacções adversas nem tão-pouco a sua gravidade de forma explícita. Em todo o caso, induz-se que as vacinas contra a covid-19 foram o principal grupo de fármacos a dar problemas nos últimos anos, porque o número total de reacções adversas classificadas como graves mais que duplicou em 2021, no auge do programa de vacinação, face aos anos anteriores. Assim, se em 2019 o Infarmed contabilizara 5.511 reacções graves e 4.482 no ano seguinte, em 2021 foram registadas 11.435, descendo depois para 6.086 em 2022 e para 5.043 no ano passado.
Se se considerar que sensivelmente metade das cerca de 28 mil mortes associadas à covid-19 ocorreram antes do processo de vacinação, a existência de tantos milhares de casos graves deveria merecer, subentende-se, uma análise atenta da entidade responsável pela farmacovigilância em Portugal, o Infarmed.
Mas isso, infelizmente, não sucedeu.
E pior: além de uma incompreensível atitude obscurantista, negando ceder a informação do Portal RAM – que somente foi desbloqueada por um acórdão do Tribunal Central Administrativo do Sul (TCAS) –, o Infarmed acaba por demonstrar que não faz farmacovigilância, e abandona à sua sorte as vítimas de reacções adversas às vacinas, contribuindo também para confundir uma avaliação correcta de custo-benefício.
Com efeito, apesar de o Infarmed insistir na recusa de revelar os dados do Portal RAM posteriores a 6 de Dezembro de 2021 – sabendo-se que o TCAS concedeu o direito de acesso, pela primeira vez, em Junho de 2024 –, e ter apagado variáveis (entre as quais a causalidade) e agregado as idades das vítimas, o PÁGINA UM analisou os casos de reacções adversas que atingiram crianças, adolescentes e jovens adultos. Uma ponta do icebergue, uma vez que, sobretudo no caso das crianças com menos de 12 anos, a vacinação ocorreu sobretudo a partir de Dezembro de 2021.
E os dados são aterradores – também muito pela inqualificável negligência do Infarmed, que, de forma despudorada e intencional, descura as suas funções básicas.
A partir da análise do PÁGINA UM ao Portal RAM até 6 de Dezembro de 2021, de entre as 27.220 reacções adversas, 513 foram de menores de 25 anos em que o Infarmed deu a classificação de grave. Destas, seis foram recém-nascidos (não vacinados), que sofreram diversas desordens (gastrointestinais, nervosas, endócrinas e de pele) por via do leite materno; 99 eram de adolescentes dos 12 aos 17 anos; e 408 eram de jovens adultos com menos de 25 anos. Este número é já em si muito significativo, atendendo à baixíssima taxa de mortalidade da covid-19 nos grupos etários jovens. Note-se que, segundo dados do INE, em três anos (2020-2022) morreram 29 pessoas com menos de 25 anos cuja causa foi atribuída à covid-19, um valor substancialmente mais baixo do que as mortes provocadas por pneumonias nessa faixa etária.

Mas a questão essencial a colocar quando se observam 513 reacções adversas graves em grupos etários tão jovens – e não esquecer que não estão incluídas as crianças dos 5 aos 12 anos, nem outros casos detectados posteriormente a 6 de Dezembro de 2021 –, a pergunta que se deve colocar de imediato é se houve mortes. E de que tipo foram e como evoluíram os casos graves? Evoluíram favoravelmente, tiveram um desfecho trágico, ficaram sequelas?
E é aqui que se nota que o Infarmed não faz farmacovigilância.
Com efeito, e fazendo nota que estes dados são oficiais e emanados após decisão de um tribunal administrativo superior – ou seja, não são ‘inventados’ pelo PÁGINA UM –, contabilizam-se 225 casos cujo desfecho é desconhecido pelo Infarmed. Ou, dizendo de outra forma, o Infarmed não quis fazer o acompanhamento – também conhecido por monitorização –, não fosse dar-se o caso de haver muitas mortes a registar por causa das ‘seguras’ vacinas.
Assim, por exemplo, o que sucedeu a um lactente, identificado como caso 23506, que chegou a ser hospitalizado com uma trombocitose suspeita de advir do leite materno, dado a sua mãe ter sido vacinada com a AstraZeneca? O Infarmed regista “Desconhecido” na base de dados, apesar de a notificação ter ocorrido em 7 de Outubro de 2021.
De igual modo, o que sucedeu à adolescente do sexo feminino (caso 19645) que teve um tromboembolismo após a toma da vacina da Pfizer em Agosto de 2021? Sabe-se que foi hospitalizada, mas apesar de esta ser uma das afectações mais graves e conhecidas associadas à vacina contra a covid-19, o Infarmed achou que não valia a pena saber como evoluiu.

E as famigeradas miocardites e pericardites? Há 10 situações classificadas como graves, entre Agosto e Outubro de 2021, cujo desfecho o Infarmed desconhece, havendo situações de registo com a mera indicação de a vítima estar “em recuperação”. Mas são casos já passados há cerca de três anos. Destes, cinco são de adolescentes (casos 19951; 22118; 22269; 22467; e 23415) e outros cinco de jovens adultos até aos 24 anos (casos 18193; 22581; 23267; 23208; e 26223).
Também surge registada a situação de uma adolescente com síndrome inflamatória multissistémica pediátrica (MIS-C) associada à vacina contra a covid-19 (caso 20713), mas apesar de ter ocorrido em Agosto de 2021, com hospitalização, surge a referência “desconhecido” no campo a evolução da reacção adversa. O Infarmed considerou que não se mostra necessário saber como evoluíram estas infecções do coração, se ficaram sequelas, se houve mortes. Nada importou para se manter o selo das vacinas seguras.
Também dúvidas ficam sobre a qualidade da farmacovigilância da entidade liderada por Rui Santos Ivo quando se observam outras situações de elevadíssima gravidade com grande risco de sequelas ou mortes. O PÁGINA UM detectou, por exemplo, registos de embolia pulmonar (caso 10215, uma jovem mulher que tomou a AstraZeneca, em Maio de 2021), de trombose venosa cerebral (caso 18886, uma jovem mulher que tomou a vacina Moderna, em Agosto de 2021), de trombocitopenia imune (caso 19516, outra jovem mulher que tomou a Moderna, em Agosto de 2021), de acidente vascular cerebral (caso 20843, um jovem adulto que tomou a vacina da Janssen, em Setembro de 2021).
E, de resto, há um significativo número de sintomas genéricos do aparelho endócrino, do sistema nervoso e da pele, incluindo também doenças ou perturbações raras (como paralisia facial ou síndrome de Parsonage-Turner), que quer ponham ou não em risco a vítima, deveriam merecer atenção do Infarmed. Até para fazer sentido, em português, a palavra ‘monitorização’. Na base de dados analisada pelo PÁGINA UM, há também diversos casos graves de perturbações do ciclo menstrual em jovens mulheres. Aliás, se incluirmos as mulheres de todas as idades, o Portal RAM registou, até início de Dezembro de 2021, cerca de duas centenas de alterações menstruais associadas às vacinas contra a covid-19.

Saliente-se também que o Infarmed decidiu manipular a base de dados que o Tribunal Administrativo Central do Sul ordenou que fosse disponibilizada ao PÁGINA UM, uma vez que apagou a variável que, para cada caso, indicasse o grau de causalidade (definitiva, provável, possível e improvável). A probabilidade de ter sido um acaso é definitivamente improvável – ou seja, houve intenção deliberada do Infarmed em esconder informação vital.
O PÁGINA UM confrontou o Infarmed, através do seu presidente Rui Santos Ivo, e a ministra da Saúde, Ana Paula Martins, com os resultados desta análise. Certamente confiantes de que esta notícia do PÁGINA UM não tenha impacte público, mesmo face à gravidade comportamental do Infarmed, nem Rui Santos Ivo nem Ana Paula Martins se dignaram reagir, confiantes na sua impunidade. Na verdade, em Portugal, para o medicamento que mais reacções adversas apresentou na moderna História da Farmacologia, vai ficar tudo bem – excepto para os ‘azarados’ que tomaram as vacinas “seguras e eficazes” e ficaram entrevados. Ou mortos. Mesmo se, desses, para as autoridades, nem um pio se quer que a História dê.
